Elektronische Unterschriften und digitale Signaturen dürfen als gleichwertig zu handgeschriebenen Unterschriften („wet ink“) betrachtet werden.
Welche Voraussetzungen dafür erfüllt sein müssen, hängt vom Grad der zu erreichenden Verbindlichkeit und damit vom Dokument ab, das unterschrieben werden soll.
Dieser Artikel klärt,
- wann
Hersteller überhaupt eine Unterschrift benötigen, - unter
welchen Umständen diese Unterschrift elektronisch erfolgen darf, - welcher
Typ an elektronischer Unterschrift verlangt wird, - was
der Unterschied zwischen einer elektronischen Unterschrift und einer digitalen
Signatur ist und - wie
sich das elektronische Signieren in der Praxis umsetzen lässt.
1. Wann benötigt man (überhaupt) eine Unterschrift?
a) Medizinprodukteverordnung MDR
Die MDR fordert explizit Unterschriften beispielsweise im Anhang IV zur „EU-Konformitätserklärung“:
„Die EU-Konformitätserklärung enthält alle folgenden Angaben: […] Ort und Datum der Ausstellung der Erklärung, Name und Funktion des Unterzeichners sowie Angabe, für wen und in wessen Namen diese Person unterzeichnet hat, Unterschrift“.
MDR, Anhang IV
Zudem müssen die Hersteller eine Unterschrift leisten, wenn sie bei einer benannten Stelle beantragen, eine Konformitätsbewertung durchzuführen. Auch bei klinischen Prüfungen fordert die MDR die Unterschriften
der „Hauptprüfer“.
Weitere Forderungen nach Unterschriften betreffen die Benannten Stellen:
- Verpflichtung der Mitarbeitenden
- Entscheidung über Zertifizierungen
- Bescheinigungen
b) IVDR
Die IVDR stellt die gleichen Anforderungen wie die MDR. Nur bei den klinischen Leistungsstudien, dem Pendent zu den klinischen Prüfungen, verzichtet die IVDR auf die Pflicht zu Unterschriften.
c) ISO 13485:2016
Die DIN EN ISO 13485:2016 erwähnt den Begriff „Unterschrift“ nicht. Allerdings verlangt sie in Kapitel 4.2.4 („Lenkung von Dokumenten“):
Ein dokumentiertes Verfahren muss die erforderlichen Lenkungsmaßnahmen festlegen, um:
a) Dokumente bezüglich ihrer Angemessenheit vor ihrer Herausgabe zu bewerten und zu genehmigen, […]DIN EN ISO 13485:2016, Kapitel 4.2.4
Damit sind die Hersteller verpflichtet nachzuweisen, dass
- Dokumente
geschrieben, bewertet und genehmigt werden, - dies
in dieser Reihenfolge geschieht, - nicht
die gleiche Person schreibt, bewertet und genehmigt und - die
Genehmigung vor der Herausgabe erfolgt.
Diese Anforderungen lassen sich nur durch eine Zuordnung des Dokuments und der Tätigkeiten zu einer Person und einem Datum für jede Tätigkeit erfüllen. Genau diese Zuordnung erfolgt bei Papier meist durch eine Unterschrift. Bei elektronischen Dokumenten und Aufzeichnungen gibt es Alternativen (s. u.).
In allen Fällen muss dokumentiert sein:
- Autorenschaft: „Ich verantworte den Inhalt und halte ihn für korrekt.“
- Bewertung / Review: „Der Inhalt wurde von mir nach festgelegten Kriterien geprüft und entspricht diesen.“
- Genehmigung / Freigabe: „Der Inhalt kann im weiteren Prozess benutzt werden (und ich habe die Befugnis, dies zu entscheiden)“
Diese Anforderungen sind nachvollziehbar: Eine Systemspezifikation zu erstellen, bevor man die User Requirements erhoben und dokumentiert hat, ergibt meist wenig Sinn. Bevor ein Produkt in der Produktion vervielfältigt wird, muss das Design in Tests überprüft worden sein.
d) Zusammenfassung
Damit können wir zusammenfassen:
- Die Hersteller sind verpflichtet, Dokumente zu erstellen wie die technische Dokumentation und die Konformitätserklärung.
- Sie müssen nur wenige dieser Dokumente unterschreiben.
- Die Unterschrift sind eher notwendig, um die Produktkonformität zu bestätigen (Konformitätserklärung), weniger für die Prozesskonformität (Aufzeichnungen, technische Dokumentation).
- Auch bei den Nachweisen der Prozesskonformität muss erkennbar sein, wer, wann welchen Arbeitsschritt (z.B. eine Freigabe) wie gemacht hat.
2. Wann benötigt man elektronische Unterschriften?
Elektronische Dokumente und Aufzeichnungen sind noch nicht überall verpflichtend. Allerdings wächst der Druck von Behörden und benannten Stellen, dies zu tun. Standardisierte elektronische Formate wie CDISC bei klinischen Prüfungen und das FDA-eStar-Programm werden zunehmend die einzige effiziente Form des Daten- und Informationsaustauschs.
Mit dem Umstieg von Papier auf elektronische Dokumente entsteht noch nicht in jedem Fall die Pflicht, handgeschriebene Unterschriften durch elektronische Unterschriften zu ersetzen. Vielmehr können die Unternehmen bewerten, ob überhaupt eine Unterschrift verpflichtend ist oder ob auch auf andere Weise in ausreichendem Maß nachverfolgt werden kann, welche Person welche Tätigkeit zu welchem Zeitpunkt durchgeführt hat.
Die Vorgaben im eigenen QM-System sind bei Änderungen anzupassen.
Mit dem Umstieg auf elektronische Medien findet zunehmend ein Wechsel von dokumenten- zu datengetriebenen Prozessen statt. Damit erfolgt ein Wechsel von Papier auf elektronische Dokumente auf strukturierte Daten.
Auch die strukturierten Daten müssen die gesetzlichen Anforderungen an die Lenkung von Dokumenten und Aufzeichnungen erfüllen.
Das Johner Institut unterstützt Hersteller und Benannte Stellen bei deren digitalen Transformation z.B. im Rahmen des Fit-for-Future-Programms.
3. Wann sind eine elektronische Unterschriften erlaubt?
a) In Deutschland / Europa: BGB, VDG, eIDAS
Das Bürgerliche Gesetzbuch BGB gibt im §126 „Schriftform“ explizit die Erlaubnis handschriftliche Unterschriften durch elektronische Unterschriften zu ersetzen:
„… (3) Die schriftliche Form kann durch die elektronische Form ersetzt werden, wenn sich nicht aus dem Gesetz ein anderes ergibt. …“
BGB, §126
Bei gesetzlich vorgeschriebenen Unterschriften hängt das BGB
die Latte noch etwas höher:
„(1) Soll die gesetzlich vorgeschriebene schriftliche Form durch die elektronische Form ersetzt werden, so muss der Aussteller der Erklärung dieser seinen Namen hinzufügen und das elektronische Dokument mit einer qualifizierten elektronischen Signatur versehen.
BGB §126a
Was eine „qualifizierte elektronische Signatur“ ist, regelt das Vertrauensdienstegesetz VDG (ehemals Signaturgesetz), welches die EU-Verordnung eIDAS (ehemals Signaturrichtlinie) umsetzt (s. Abb. 1).
b) USA – FDA: 21 CFR part 11
Die FDA gestattet ebenfalls den Ersatz von schriftlichen
durch elektronische Unterschriften. Die Unterschriften und die damit
unterzeichneten Dokumente müssen dann den Anforderungen des 21 CFR part 11
genügen.
Die Anforderungen dieses administrativen Gesetzes gelten nur
für Firmen, die mit der FDA kommunizieren bzw. der Behörde Dokumente vorlegen müssen
z.B. während einer Inspektion.
4. Welche Typen an elektronischen Unterschriften gibt es?
Die EU-Verordnung über elektronische Identifizierung und
Vertrauensdienste (kurz eIDAS (910/2014)) unterscheidet drei Typen an
elektronischen Unterschriften:
- Elektronische
Signatur - Fortgeschrittene
elektronische Signatur - Qualifizierte
elektronische Signatur
a) Elektronische Signatur
Die eIDAS definiert eine elektronische Signatur wie folgt:
„Daten in elektronischer Form, die anderen elektronischen Daten beigefügt oder logisch mit ihnen verbunden werden und die der Unterzeichner zum Unterzeichnen verwendet.“
Quelle: eIDAS
Das Einfügen eines Unterschriften-Scans in ein Dokument ist
ein Beispiel für eine elektronische Signatur. Ebenso ist die Signatur in einer
E-Mail eine elektronische Signatur.
Diese Signatur stellt die schwächste Form des Nachweises
statt, da weder sichergestellt ist, dass die Person selbst diese „Daten
beigefügt oder logisch verbunden“ hat, noch lässt sich der Zeitpunkt dieses Beifügens
nachvollziehen.
b) Fortgeschrittene elektronische Signatur
Die nächste Stufe sind die fortgeschrittenen elektronischen
Signaturen.
elektronische Signaturen nach Nummer 1, die
- eindeutig dem Unterzeichner zugeordnet sind,
- die Identifizierung des Unterzeichners ermöglichen,
- unter Verwendung elektronischer Signaturerstellungsdaten erstellt sind, die der Unterzeichner mit einem hohen Maß an Vertrauen unter seiner alleinigen Kontrolle verwenden kann, und
- so mit den auf diese Weise unterzeichneten Daten verbunden sind, dass eine nachträgliche Veränderung der Daten erkannt werden kann
Quelle: eIDAS
Ein Beispiel für diesen Typ an elektronischen Unterschriften sind Versionsverwaltungssysteme wie SVN oder git:
- Beim „Commit“ wird immer der Name der Person und der Zeitpunkt mit gespeichert.
- Durch seinen Benutzernamen und sein Passwort kann die Person identifiziert werden.
- Organisatorisch lässt sich sicherstellen, dass nur die Person selbst über diese „Credentials“ verfügt.
- Schließlich stellen Prüfsummen sicher, dass eine nachträgliche Veränderung der Daten nicht unbemerkt bliebe.
Genau dazu sind Versionsverwaltungssysteme gedacht.
Aber auch fortgeschrittene elektronische Signaturen bieten
die Möglichkeit der Manipulation:
- Wenn
die organisatorischen Maßnahmen nicht wirksam sind, wäre es möglich, dass eine
zweite Person den gleichen Namen verwendet oder dass sie Zugriff zu Zugangsdaten
und damit die Identität der ersten Person erlangt. - Durch
ein Verändern der Systemzeit des Versionsverwaltungssystems ließe sich der
Zeitstempel manipulieren.
Um diese Nachteile zu minimieren, bedarf es ggf. einem
höheren „Integritätslevel“, der qualifizierten elektronischen Signatur.
Viele Dienstleister von elektronischen Signaturen bieten „nur“ fortgeschrittene Signaturen an. Dennoch werden damit in der Praxis auch umfangreiche Vertragswerke unterzeichnet.
c) Qualifizierte elektronische Signatur
Auch diesen Typ definiert eIDAS:
„Fortgeschrittene elektronische Signaturen nach Nummer 2, die
- von einer qualifizierten elektronischen Signaturerstellungseinheit erstellt wurden und
- Auf einem qualifizierten Zertifikat für elektronische Signaturen beruhen-
Quelle: eIDAS
Im Anhang II ergänzt die Verordnung:
„(3) Das Erzeugen oder Verwalten von elektronischen Signaturerstellungsdaten im Namen eines Unterzeichners darf nur von einem qualifizierten Vertrauensdiensteanbieter durchgeführt werden.“
Quelle: eIDAS
Zu diesen Anbietern zählen:
- Bundesagentur für Arbeit
- Bundesnotarkammer
- Deutsche Post AG
- D-Trust GmbH
- Deutscher Sparkassen Verlag GmbH
- Deutsche Telekom AG
- DGN Deutsches Gesundheitsnetz Service GmbH
- medisign GmbH
5. Welchen Typ an elektronischer Signatur benötigt man?
a) Risikobasierter Ansatz der ISO 13485:2016
Die ISO 13485:2016 spricht davon, dass Prozesse und die Validierung von Computersystemen risikobasiert erfolgen sollen. Diesen risikobasierten Ansatz gilt es, auch bei der Wahl des Typs an elektronischer Signatur anzuwenden.
Wenn es um Menschenleben geht (> Produktkonformität), wird man auf das höchste Niveau wählen. Wenn es um den Nachweis geht, dass man seinen Verfahrensanweisungen gefolgt ist (> Prozesskonformität), sollte eine fortgeschrittene elektronische Signatur genügen.
In anderen Worten: Eine Konformitätserklärung sollten
Hersteller von Hand („wet ink“) oder mit einer qualifizierten elektronischen
Signatur unterschreiben. Bei Spezifikationen, Testberichte u.ä. genügt eine
fortgeschrittene elektronische Signatur.
b) Rechtliche Anforderungen in Europa
Die eIDAS stellt explizit klar:
„(1) Einer elektronischen Signatur darf die Rechtswirkung und die Zulässigkeit als Beweismittel in Gerichtsverfahren nicht allein deshalb abgesprochen werden, weil sie in elektronischer Form vorliegt oder weil sie die Anforderungen an qualifizierte elektronische Signaturen nicht erfüllt.“
eIDAS
c) Rechtliche Anforderungen in den USA
Der 21 CFR part 11 unterscheidet die elektronische und die digitale Signatur:
(5) Digital signature means an electronic signature based upon cryptographic methods of originator authentication, computed by using a set of rules and a set of parameters such that the identity of the signer and the integrity of the data can be verified.
(7) Electronic signature means a computer data compilation of any symbol or series of symbols executed, adopted, or authorized by an individual to be the legally binding equivalent of the individual’s handwritten signature.
21 CFR part 11
Die elektronische Signatur entspricht der elektronischen
Signatur gemäß eIDAS, die digitale Signatur zumindest der fortgeschrittenen
elektronischen Signatur.
Die FDA stellt keine Anforderungen, die nur durch eine
qualifizierte elektronische Signatur erfüllt werden könnten. Sie fordert:
- Verfälschungen müssen erkannt werden (11.10)
- Angemessene Standards für digitale Signaturen, um die Authentizität, Integrität und Vertraulichkeit von Aufzeichnungen zu gewährleisten (11.30)
- Sicherstellung, dass Unterschriften nicht entfernt oder auf andere Dokumente übertragen werden können (11.70)
- Will eine Person mehrere elektronische Unterschriften leisten, muss sie sich initial mit allen Daten anmelden (typischerweise Benutzername und Passwort), dann für jeden einzelnen Vorgang mit mindestens einer Komponente (typischerweise Passwort oder PIN) (11.200)
- Sicherstellung, dass es das Zusammenwirken zweiter Personen bedürfte, um die elektronische Unterschrift einer dritten Person zu fälschen. (11.200)
- Auf einem elektronisch unterschriebenen Dokument erwartet die FDA den Namen des Unterzeichners (in Druckbuchstaben, kein Bild/Scan der Unterschrift), Datum und Uhrzeit der Unterschrift und was mit der Unterschrift bestätigt wird (Autorenschaft, Prüfung, Freigabe) (11.50). Diese Unterschrift kann bei Dokumenten, die in Systemen „leben“ (z.B. einem ALM Tool) auch im System hinterlegt sein, die technisch untrennbar mit dem Inhalt des Dokuments verknüpft ist.
Fazit: Keine dieser Anforderungen macht es zwingend, qualifizierte elektronische Unterschriften zu verwenden. Eine fortgeschrittene elektronische Unterschrift mit einem validierten System gepaart mit geeigneten organisatorischen Maßnahmen sind ausreichend.
6. Wie (mit welchen Werkzeugen) erstellt man eine digitale Unterschrift?
Das Johner Institut empfiehlt, Werkzeuge zu nutzen, um
digitale Unterschriften zu leisten. Die Art der geeigneten Werkzeuge hängt von
der Arbeitsweise der Hersteller ab:
- Wenn Hersteller vor allem dokumentenorientiert arbeiten (z.B. mit Word), sind die Produkte von Adobe und Microsoft (z.B. Word) alleine bzw. mit Plugins ausreichend, um die technischen Voraussetzungen an eine fortgeschrittene elektronische Signatur zu erfüllen.
- Das Johner Institut selbst erstellt die meisten Dokumente im Markdown-Format und nutzt git als Versionsverwaltungswerkzeug. Durch geeignete organisatorische Maßnahmen (z.B. Vorgaben zum Branching und Merging) lassen sich die Anforderungen an eine fortgeschrittene elektronische Signatur erfüllen.
- Sehr elegant ist es, auf Werkzeuge zu setzen, die die Inhalte der Dokumente in einer Datenbank pflegen wie die ALM-Tools z.B. die von Medsoto (MedPack, RiskPack und Polarion ALM). Diese Produkte verfügen bereits über eingebaute Mechanismen wie z.B. die Bestätigung von Freigaben per Passwort, um rechtskonforme fortgeschrittene elektronische Signaturen zu erzeugen.
Das Unterschreiben von Konformitätserklärungen rechtfertig den Aufwand meist nicht, ein System zu etablieren, mit dem qualifizierte elektronische Signaturen erzeugt werden können.
Sven Wittorf, der Geschäftsführer unseres Schwesterunternehmens Medsoto hat sich die Mühe gemacht, die Voraussetzungen für eine qualifizierte digitale Signatur zu schaffen. Hier ist sein (Leidens-)Bericht:
7. Wie funktioniert das digitale Signieren technisch?
a) Digitale Signatur: Was hat das mit Hashwert z.B. MD5 und SHA zu tun?
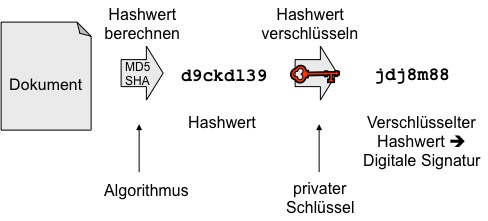
Zuerst wird aus dem Dokument ein so genannter Hashwert
berechnet. Der Hashwert ist eine Zeichenkette (aktuell meist 254 Bit oder
länger) und gleicht einem Fingerabdruck des Dokuments. Jede auch noch so kleine
Änderung an dem Dokument wird bei einer Prüfung zu einem anderen Hashwert
führen. Es ist (mit realistischem Aufwand) nicht möglich, aus dem Hashwert auf
den Inhalt des Dokuments Rückschlüsse zu ziehen.
Bekannte und heute noch genutzte Verfahren (Algorithmen) zur
Berechnung dieses Wertes sind MD5 (128 Bit), SHA-256, und SHA-512. Das BSI gibt
jedes Jahr diesbezügliche Empfehlungen heraus, die mit Experten abgestimmt
sind.
Typische Längen für eine digitale Signatur sind 1536
Bit und mehr. Da die Hash-Algorithmen deutlich kürzere Zeichenketten ergeben,
werden diese dann durch spezielle Zeichen aufgefüllt. Dieser Vorgang wird
Padding genannt.
b) Verschlüsselung, RSA und digitale Signatur
Soweit sind weder das Originaldokument noch dessen Hashwert
einem Urheber zuordenbar. Dies erfolgt im zweiten Schritt dadurch, dass der
(aufgefüllte) Hashwert durch ein Signaturverfahren mit dem privaten Schlüssel
des Urhebers zu einer Signatur verknüpft wird. Weit verbreitete, asymmetrische
Verfahren dafür sind RSA bzw. DSA.
Wohlgemerkt: Für Signaturzwecke wird der Hashwert und nicht
das komplette Dokument mit dem Schlüssel verknüpft, weil hierfür nicht der
Inhalt des Dokuments verborgen, sondern „nur“ dessen Integrität gewährleistet
werden soll. Der Hashwert stellt somit eine wesentliche Komponente der
digitalen Signatur dar.
Auch für Signatur und Verschlüsselung analysiert das BSI jährlich die Sicherheit der empfohlenen Verfahren. Eine auf RSA bzw. DSA basierende Signatur mit einer Länge von 2000 Bit wird bis 2022 als sicher angesehen. Danach sind mindestens 3000 Bit erforderlich (Quelle).
c) Schlüssel, Zertifikat und Zertifizierungsstelle
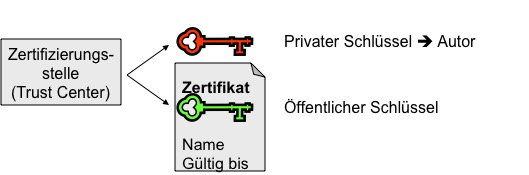
Dass der Schlüssel wirklich vertrauenswürdig dem Urheber
zugeordnet werden kann, belegen Zertifikate. Sie werden von Trust-Centern
(Zertifizierungsinstanzen) ausgestellt, sind von dieser signiert (und damit
integer) und enthalten neben dem Namen des Urhebers und dem Fälligkeitsdatum
auch dessen öffentlichen Schlüssel. Öffentlicher und privater Schlüssel bilden
dabei ein Paar. Während der öffentliche Schlüssel aus dem privaten Schlüssel
erzeugt wird, ist dies umgekehrt nicht möglich, d.h. aus dem öffentlichen
Schlüssel lässt sich der private Schlüssel nicht ermitteln. Auf dem Prinzip einer
solchen „Einwegfunktion“ beruht die Sicherheit des Verfahrens.
Mit dem öffentlichen Schlüssel aus dem Zertifikat des
potenziellen Senders kann der Empfänger die dem Dokument beigefügte digitale
Signatur verifizieren und damit die Korrektheit der Angaben zum Urheber (Autor
bzw. Sender) prüfen. Dabei wird auch der gespeicherte Hashwert sichtbar. Den
entschlüsselten Wert vergleicht der Empfänger danach mit dem Hashwert, den er
selbst unter Anwendung des gleichen Algorithmus berechnet hat. Stimmen beide
überein, so weiß der Empfänger sicher, dass das Dokument unverändert und damit
auch authentisch ist.
8. Fazit / Zusammenfassung
a) Unnötigen Aufwand vermeiden
Den Aufwand, den einige Firmen treiben, um angebliche gesetzliche
Anforderungen zu erfüllen, treibt seltsame Blüten: Man erzeugt elektronische Dokumente.
Dann druckt man diese aus. Anschließend unterschreibt man sie und scannt sie
wieder ein. Dieser Scan wandert dann zur Archivierung in ein
Dokumentenmanagementsystem, das mit einem aufwändigen Berechtigungsprozess
sicherstellt, dass die Personen identifiziert werden können, die damit arbeiten.
Es ist ein leichtes, die Prozesseffizienz durch unangemessen
hohe Vorgaben zu beeinträchtigen und damit die ganze Firma stillzulegen.
b) Zukunftssicher handeln
Die digitale Transformation von Medizinprodukteherstellern, Behörden und Benannten Stellen gelingt nicht durch einen Umstieg von Papier auf elektronische Dokumente. Vielmehr ist ein Umstieg von Dokumenten auf strukturierte Daten notwendig, um (regulatorische) Prozesse zu automatisieren.
Die dafür verwendeten Systeme müssen die Anforderungen insbesondere der ISO 13485 an die Lenkung von Dokumenten und Aufzeichnungen erfüllen, selbst wenn gar keine (elektronischen) Dokumente mehr bestehen.
Das Johner Institut hilft Herstellern damit, insbesondere regulatorische Prozesse zu automatisieren, um
- Regulatory Affairs und Quality Managers von Fleißarbeiten zu entlasten,
- die Time-to-Market drastisch zu reduzieren,
- regulatorische Risiken zu minimieren und
- die Wettbewerbsfähigkeit und Arbeitsplatzsicherheit zu gewährleisten.
Melden Sie sich bei Interesse z.B. über die Kontaktseite.
c) Risikobasiert handeln
Die Wahl des Signatur-Niveaus sollte risikobasiert erfolgen: Eine qualifizierte elektronische Signatur empfiehlt das Johner Institut v.a. für Konformitätserklärungen („es geht um Leben und Tod“) und externe Rechtsgeschäfte. In den anderen Fällen genügt eine fortgeschrittene elektronische Signatur, wie Sie sich mit vielen Tools erstellen können, zusammen mit geeigneten organisatorischen Maßnahmen.
Manche Auditoren stellen bezüglich elektronischer Unterschriften Anforderungen, für die es keine rechtliche Basis gilt. Diese Auditoren handeln meist inkonsistent, denn sie bestehen bei handschriftlichen Unterschriften auch nicht auf einer Unterschriftenprobe.
Bei aller Begeisterung für elektronische Unterschriften und
für die Digitalisierung: Ist es nicht auch ein feierlicher Akt, mit einem
richtigen Füller die Konformitätserklärung zu unterschreiben und zu bestätigen,
dass das Produkt sicher ist und den Patienten nutzen wird?
Dank gilt Sven Wittorf für sehr wertvolle Anregungen und Materialien!
Änderungshistorie:
- 2024-07-29:
- Redaktionelle Änderungen
- Kapitel 1 aktualisiert u.a. MDD entfernt und IVDR ergänzt
- Kapitel 2 neu geschrieben
- Kapitel 8.c) eingefügt
- 2019-04-19: Artikel überarbeitet und um eIDAS-Anforderungen ergänzt



